Recettore nucleare - Nuclear receptor

Nel campo della biologia molecolare , i recettori nucleari sono una classe di proteine presenti all'interno delle cellule responsabili del rilevamento degli ormoni steroidei e tiroidei e di alcune altre molecole. In risposta, questi recettori lavorano con altre proteine per regolare l' espressione di geni specifici , controllando così lo sviluppo , l' omeostasi e il metabolismo dell'organismo.
I recettori nucleari hanno la capacità di legarsi direttamente al DNA e regolare l'espressione dei geni adiacenti; quindi questi recettori sono classificati come fattori di trascrizione . La regolazione dell'espressione genica da parte dei recettori nucleari avviene generalmente solo quando è presente un ligando, una molecola che influenza il comportamento del recettore. Più specificamente, il legame del ligando a un recettore nucleare determina un cambiamento conformazionale nel recettore, che, a sua volta, attiva il recettore, con conseguente up- o down-regulation dell'espressione genica.
Una proprietà unica dei recettori nucleari che li differenzia dalle altre classi di recettori è la loro capacità di interagire e controllare direttamente l'espressione del DNA genomico . Di conseguenza, i recettori nucleari svolgono ruoli chiave sia nello sviluppo embrionale che nell'omeostasi degli adulti. Come discusso di seguito, i recettori nucleari possono essere classificati secondo il meccanismo o l' omologia .
Distribuzione delle specie
I recettori nucleari sono specifici dei metazoi (animali) e non si trovano nei protisti , nelle alghe , nei funghi o nelle piante. Tra i primi-branching linee animali con genomi sequenziati, due sono stati riportati durante la spugna Amphimedon queenslandica , due dalla ctenoforo Mnemiopsis leidyi quattro dalla placozoan Trichoplax adhaerens e 17 dal cnidarian vectensis Nematostella . Ci sono 270 recettori nucleari nel solo nematode C. elegans , 21 in D. melanogaster e altri insetti, 73 in zebrafish . Umani, topi e ratti hanno rispettivamente 48, 49 e 47 recettori nucleari ciascuno.
ligandi
I ligandi che si legano ai recettori nucleari e li attivano includono sostanze lipofile come ormoni endogeni , vitamine A e D e ormoni xenobiotici . Poiché l'espressione di un gran numero di geni è regolata da recettori nucleari, i ligandi che attivano questi recettori possono avere effetti profondi sull'organismo. Molti di questi geni regolati sono associati a varie malattie, il che spiega perché i bersagli molecolari di circa il 13% dei farmaci approvati dalla Food and Drug Administration (FDA) degli Stati Uniti colpiscono i recettori nucleari.
Un certo numero di recettori nucleari, indicati come recettori orfani , non hanno ligandi endogeni noti (o almeno generalmente concordati). Alcuni di questi recettori come FXR , LXR e PPAR legano un numero di intermedi metabolici come acidi grassi, acidi biliari e/o steroli con affinità relativamente bassa. Questi recettori quindi possono funzionare come sensori metabolici. Altri recettori nucleari, come CAR e PXR, sembrano funzionare come sensori xenobiotici che aumentano l'espressione degli enzimi del citocromo P450 che metabolizzano questi xenobiotici.
Struttura
La maggior parte dei recettori nucleari ha masse molecolari comprese tra 50.000 e 100.000 dalton .
I recettori nucleari hanno una struttura modulare e contengono i seguenti domini :
- (AB) Dominio regolatorio N-terminale : Contiene la funzione di attivazione 1 ( AF-1 ) la cui azione è indipendente dalla presenza di ligando. L'attivazione trascrizionale di AF-1 è normalmente molto debole, ma si sinergizza con AF-2 nel dominio E (vedi sotto) per produrre una sovraregolazione più robusta dell'espressione genica. Il dominio AB è molto variabile in sequenza tra i vari recettori nucleari.
- (C) Dominio legante il DNA ( DBD ): Dominio altamente conservato contenente due dita di zinco che si lega a specifiche sequenze di DNA chiamate elementi di risposta ormonale (HRE). Recentemente, un nuovo motivo a dito di zinco (CHC2) è stato identificato nei parassiti NR dei platelminti.
- (D) Regione cerniera: pensato per essere un dominio flessibile che collega il DBD con il LBD. Influenza il traffico intracellulare e la distribuzione subcellulare con una sequenza peptidica bersaglio .
- (E) Dominio di legame del ligando ( LBD ): moderatamente conservato in sequenza e altamente conservato nella struttura tra i vari recettori nucleari. La struttura del LBD è indicata come una piega a sandwich alfa elicoidale in cui tre alfa eliche anti parallele (il "ripieno a sandwich") sono affiancate da due alfa eliche da un lato e tre dall'altro (il "pane"). La cavità di legame del ligando si trova all'interno del LBD e appena al di sotto di tre "riempimenti" di sandwich alfa elicoidale antiparallelo. Insieme al DBD, il LBD contribuisce all'interfaccia di dimerizzazione del recettore e, inoltre, lega le proteine del coattivatore e del corepressore . Il LBD contiene anche la funzione di attivazione 2 ( AF-2 ) la cui azione è dipendente dalla presenza di ligando legato, controllato dalla conformazione dell'elica 12 (H12).
- (F) Dominio C-terminale : Altamente variabile in sequenza tra vari recettori nucleari.
I domini N-terminale (A/B), di legame al DNA (C) e di legame al ligando (E) sono indipendentemente ben piegati e strutturalmente stabili mentre la regione cerniera (D) e i domini C-terminale (F) opzionali possono essere conformazionalmente flessibile e disordinato. Gli orientamenti relativi dei domini sono molto diversi confrontando tre strutture cristalline multidominio note, due delle quali si legano a DR1 (DBD separati da 1 bp), una si lega a DR4 (di 4 bp).

Organizzazione strutturale dei recettori nucleari In
alto – Sequenza schematica di amminoacidi 1D di un recettore nucleare. In basso – Strutture 3D delle regioni DBD (legata al DNA) e LBD (legata all'ormone) del recettore nucleare. Le strutture mostrate sono del recettore degli estrogeni . Le strutture sperimentali del dominio N-terminale (A/B), della regione cerniera (D) e del dominio C-terminale (F) non sono state determinate, pertanto sono rappresentate rispettivamente da linee tratteggiate rosse, viola e arancioni. |
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Meccanismo di azione
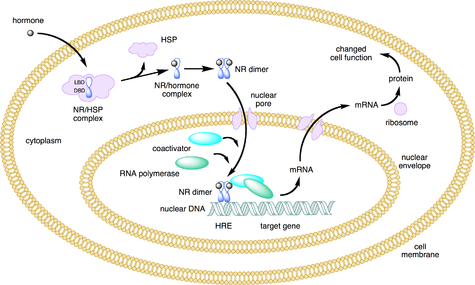

I recettori nucleari sono proteine multifunzionali che trasducono i segnali dei loro ligandi affini . I recettori nucleari (NR) possono essere classificati in due grandi classi in base al loro meccanismo d'azione e alla distribuzione subcellulare in assenza di ligando.
Piccole sostanze lipofile come gli ormoni naturali si diffondono attraverso la membrana cellulare e si legano ai recettori nucleari situati nel citosol (tipo I NR) o nel nucleo (tipo II NR) della cellula. Il legame provoca un cambiamento conformazionale nel recettore che, a seconda della classe del recettore, innesca una cascata di eventi a valle che dirigono gli NR ai siti di regolazione della trascrizione del DNA che determinano una regolazione verso l'alto o verso il basso dell'espressione genica. In genere funzionano come omo/eterodimeri. Inoltre, sono state identificate anche due classi aggiuntive, il tipo III che sono una variante del tipo I e il tipo IV che legano il DNA come monomeri.
Di conseguenza, i recettori nucleari possono essere suddivisi nelle seguenti quattro classi meccanicistiche:
Tipo I
Ligando di tipo I recettori nucleari nei risultati citosol nella dissociazione di proteine da shock termico , omo dimerizzazione , traslocazione ( cioè , trasporto attivo ) dal citoplasma nel nucleo cellulare e legandosi a sequenze specifiche di DNA noti come elemento di risposta all'ormone (HRE). I recettori nucleari di tipo I si legano agli HRE costituiti da due semisiti separati da una lunghezza variabile di DNA e il secondo semisito ha una sequenza invertita rispetto al primo (ripetizione invertita). I recettori nucleari di tipo I includono membri della sottofamiglia 3, come il recettore degli androgeni , i recettori degli estrogeni , il recettore dei glucocorticoidi e il recettore del progesterone .
È stato notato che alcuni dei recettori nucleari della sottofamiglia NR 2 possono legarsi a HRE a ripetizione diretta invece che a ripetizione invertita . Inoltre, alcuni recettori nucleari si legano come monomeri o dimeri, con un solo dominio di legame al DNA del recettore che si lega a un singolo mezzo sito HRE. Questi recettori nucleari sono considerati recettori orfani , poiché i loro ligandi endogeni sono ancora sconosciuti.
Il complesso recettore nucleare/DNA recluta quindi altre proteine che trascrivono il DNA a valle dell'HRE nell'RNA messaggero e infine nella proteina , che provoca un cambiamento nella funzione cellulare.
Tipo II
I recettori di tipo II, contrariamente al tipo I, sono trattenuti nel nucleo indipendentemente dallo stato di legame del ligando e inoltre si legano come eterodimeri (di solito con RXR ) al DNA. In assenza di ligando, i recettori nucleari di tipo II sono spesso complessati con proteine corepressor . Il legame del ligando al recettore nucleare provoca la dissociazione del corepressore e il reclutamento di proteine coattivatrici . Ulteriori proteine, inclusa l' RNA polimerasi, vengono quindi reclutate nel complesso NR/DNA che trascrive il DNA in RNA messaggero.
Tipo II recettori nucleari comprendono principalmente sottofamiglia 1, per esempio il recettore dell'acido retinoico , recettore retinoide X e recettore degli ormoni tiroidei .
Tipo III
I recettori nucleari di tipo III (principalmente sottofamiglia NR 2) sono simili ai recettori di tipo I in quanto entrambe le classi si legano al DNA come omodimeri. Tuttavia, i recettori nucleari di tipo III, in contrasto con il tipo I, si legano alla ripetizione diretta anziché alle HRE a ripetizione invertita .
Tipo IV
I recettori nucleari di tipo IV si legano come monomeri o dimeri, ma solo un singolo dominio di legame al DNA del recettore si lega a un singolo mezzo sito HRE. Esempi di recettori di tipo IV si trovano nella maggior parte delle sottofamiglie NR.
dimerizzazione
I recettori nucleari umani sono in grado di dimerizzare con molti altri recettori nucleari (dimerizzazione omotipica), come è stato dimostrato da esperimenti Y2H su larga scala e dagli sforzi di text mining della letteratura che si sono concentrati su interazioni specifiche. Tuttavia, esiste una specificità, con membri della stessa sottofamiglia che hanno partner di dimerizzazione NR molto simili e la rete di dimerizzazione sottostante ha alcune caratteristiche topologiche, come la presenza di hub altamente connessi (RXR e SHP).
Proteine coregolatrici
I recettori nucleari legati agli elementi della risposta ormonale reclutano un numero significativo di altre proteine (denominate coregolatori della trascrizione ) che facilitano o inibiscono la trascrizione del gene bersaglio associato nell'mRNA. La funzione di questi coregolatori è varia e comprende il rimodellamento della cromatina (rendendo il gene bersaglio più o meno accessibile alla trascrizione) o una funzione ponte per stabilizzare il legame di altre proteine coregolatorie. I recettori nucleari possono legarsi specificamente a un certo numero di proteine coregolatrici e quindi influenzare i meccanismi cellulari di trasduzione del segnale sia direttamente che indirettamente.
Coattivatori
Il legame dei ligandi agonisti (vedi sezione sotto) ai recettori nucleari induce una conformazione del recettore che lega preferenzialmente le proteine coattivatrici . Queste proteine hanno spesso un'attività intrinseca dell'istone acetiltransferasi (HAT), che indebolisce l'associazione degli istoni al DNA e quindi promuove la trascrizione genica.
Corepressori
Il legame dei ligandi antagonisti ai recettori nucleari induce invece una conformazione del recettore che lega preferenzialmente le proteine corepressor . Queste proteine, a loro volta, reclutano l' istone deacetilasi (HDAC), che rafforza l'associazione degli istoni al DNA e quindi reprime la trascrizione genica.
Agonismo vs antagonismo
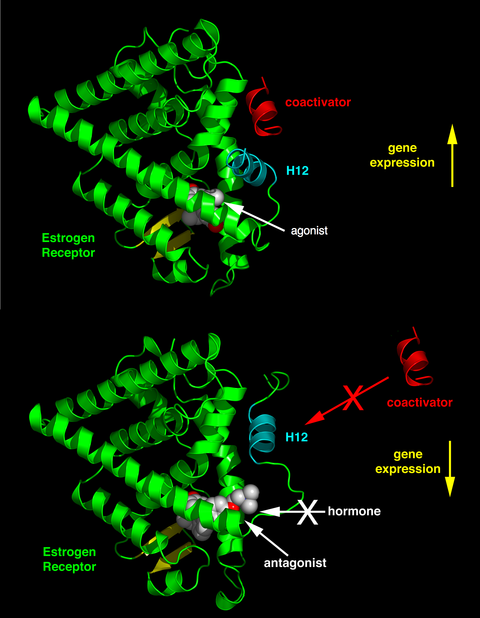
A seconda del recettore coinvolto, della struttura chimica del ligando e del tessuto interessato, i ligandi dei recettori nucleari possono mostrare effetti drammaticamente diversi che vanno dall'agonismo all'antagonismo all'agonismo inverso.
agonisti
L'attività dei ligandi endogeni (come gli ormoni estradiolo e testosterone ) quando legati ai loro recettori nucleari affini è normalmente quella di sovraregolare l'espressione genica. Questa stimolazione dell'espressione genica da parte del ligando viene definita risposta agonista . Gli effetti agonistici degli ormoni endogeni possono anche essere imitati da alcuni ligandi sintetici, ad esempio il desametasone, un farmaco antinfiammatorio del recettore dei glucocorticoidi . I ligandi agonisti agiscono inducendo una conformazione del recettore che favorisce il legame del coattivatore (vedi metà superiore della figura a destra).
Antagonisti
Altri ligandi sintetici del recettore nucleare non hanno alcun effetto apparente sulla trascrizione genica in assenza di ligando endogeno. Tuttavia bloccano l'effetto dell'agonista attraverso il legame competitivo allo stesso sito di legame nel recettore nucleare. Questi ligandi sono indicati come antagonisti. Un esempio di farmaco antagonista del recettore nucleare è il mifepristone che si lega ai recettori glucocorticoidi e progesterone e quindi blocca l'attività degli ormoni endogeni cortisolo e progesterone rispettivamente. I ligandi antagonisti agiscono inducendo una conformazione del recettore che impedisce il coattivatore e promuove il legame del corepressore (vedi metà inferiore della figura a destra).
Agonisti inversi
Infine, alcuni recettori nucleari promuovono un basso livello di trascrizione genica in assenza di agonisti (detta anche attività basale o costitutiva). I ligandi sintetici che riducono questo livello basale di attività nei recettori nucleari sono noti come agonisti inversi .
Modulatori selettivi dei recettori
Un certo numero di farmaci che agiscono attraverso i recettori nucleari mostrano una risposta agonista in alcuni tessuti e una risposta antagonista in altri tessuti. Questo comportamento può avere benefici sostanziali poiché può consentire di mantenere gli effetti terapeutici benefici desiderati di un farmaco riducendo al minimo gli effetti collaterali indesiderati. I farmaci con questo profilo d'azione misto agonista/antagonista sono indicati come modulatori selettivi dei recettori (SRM). Gli esempi includono modulatori selettivi del recettore degli androgeni ( SARM ), modulatori selettivi del recettore degli estrogeni ( SERM ) e modulatori selettivi del recettore del progesterone ( SPRM ). Il meccanismo d'azione degli SRM può variare a seconda della struttura chimica del ligando e del recettore coinvolto, tuttavia si pensa che molti SRM agiscano promuovendo una conformazione del recettore che sia strettamente bilanciata tra agonismo e antagonismo. Nei tessuti in cui la concentrazione di proteine coattivatrici è superiore a quella dei corepressori , l'equilibrio è spostato nella direzione dell'agonista. Al contrario nei tessuti in cui dominano i corepressori , il ligando si comporta come un antagonista.
Meccanismi alternativi
transrepressione
Il meccanismo più comune di azione del recettore nucleare prevede il legame diretto del recettore nucleare con un elemento di risposta dell'ormone del DNA. Questo meccanismo è denominato transattivazione . Tuttavia alcuni recettori nucleari non solo hanno la capacità di legarsi direttamente al DNA, ma anche ad altri fattori di trascrizione. Questo legame spesso porta alla disattivazione del secondo fattore di trascrizione in un processo noto come transrepressione . Un esempio di recettore nucleare in grado di transreprimere è il recettore dei glucocorticoidi (GR). Inoltre, alcuni ligandi GR noti come agonisti selettivi del recettore dei glucocorticoidi ( SEGRA ) sono in grado di attivare GR in modo tale che GR transreprima più fortemente che transattiva. Questa selettività aumenta la separazione tra gli effetti antinfiammatori desiderati e gli effetti collaterali metabolici indesiderati di questi glucocorticoidi selettivi .
Non genomico
I classici effetti diretti dei recettori nucleari sulla regolazione genica normalmente richiedono ore prima che si veda un effetto funzionale nelle cellule a causa del gran numero di passaggi intermedi tra l'attivazione del recettore nucleare e le variazioni dei livelli di espressione proteica. Tuttavia è stato osservato che molti effetti dell'applicazione di ormoni nucleari, come i cambiamenti nell'attività del canale ionico, si verificano in pochi minuti, il che è incompatibile con il meccanismo classico dell'azione del recettore nucleare. Mentre il bersaglio molecolare per questi effetti non genomici dei recettori nucleari non è stato dimostrato in modo conclusivo, è stato ipotizzato che ci siano varianti di recettori nucleari che sono associati alla membrana invece di essere localizzati nel citosol o nel nucleo. Inoltre, questi recettori associati alla membrana funzionano attraverso meccanismi di trasduzione del segnale alternativi che non coinvolgono la regolazione genica.
Sebbene sia stato ipotizzato che ci siano diversi recettori associati alla membrana per gli ormoni nucleari, è stato dimostrato che molti degli effetti rapidi richiedono recettori nucleari canonici. Tuttavia, testare l'importanza relativa dei meccanismi genomici e non genomici in vivo è stato impedito dall'assenza di meccanismi molecolari specifici per gli effetti non genomici che potrebbero essere bloccati dalla mutazione del recettore senza interrompere i suoi effetti diretti sull'espressione genica.
Un meccanismo molecolare per la segnalazione non genomica attraverso il recettore nucleare dell'ormone tiroideo TRβ coinvolge la fosfatidilinositolo 3-chinasi ( PI3K ). Questa segnalazione può essere bloccata da una singola sostituzione da tirosina a fenilalanina in TRβ senza interrompere la regolazione genica diretta. Quando i topi sono stati creati con questa singola sostituzione conservativa di amminoacidi in TRβ, la maturazione sinaptica e la plasticità nell'ippocampo sono state compromesse quasi con la stessa efficacia del blocco della sintesi dell'ormone tiroideo. Questo meccanismo sembra essere conservato in tutti i mammiferi ma non nei TRα o in altri recettori nucleari. Pertanto, l'associazione fosfotirosina-dipendente di TRβ con PI3K fornisce un potenziale meccanismo per integrare la regolazione dello sviluppo e del metabolismo da parte dell'ormone tiroideo e del recettore tirosina chinasi. Inoltre, la segnalazione dell'ormone tiroideo attraverso PI3K può alterare l'espressione genica.
Membri della famiglia
Quello che segue è un elenco dei 48 recettori nucleari umani conosciuti (e dei loro ortologhi in altre specie) classificati in base all'omologia di sequenza . L'elenco include anche membri della famiglia selezionati privi di ortologhi umani (simbolo NRNC evidenziato in giallo).
| sottofamiglia | Gruppo | Membro | ||||||
|---|---|---|---|---|---|---|---|---|
| Simbolo NRNC | Abbreviazione | Nome | Gene | ligando(i) | ||||
| 1 | Simile al recettore dell'ormone tiroideo | UN | Recettore dell'ormone tiroideo | NR1A1 | TRα | Recettore dell'ormone tiroideo-α | THRA | Ormone della tiroide |
| NR1A2 | TR | Recettore dell'ormone tiroideo-β | THRB | |||||
| B | Recettore dell'acido retinoico | NR1B1 | RARα | Recettore dell'acido retinoico-α | RARA | vitamina A e composti correlati | ||
| NR1B2 | RARβ | Recettore dell'acido retinoico-β | RARB | |||||
| NR1B3 | RARγ | Recettore dell'acido retinoico-γ | RARG | |||||
| C | Recettore attivato dal proliferatore dei perossisomi | NR1C1 | PPARα | Recettore-α . attivato dal proliferatore dei perossisomi | PARA | acidi grassi , prostaglandine | ||
| NR1C2 | PPAR-β/δ | Recettore-β/δ . attivato dal proliferatore dei perossisomi | PPARD | |||||
| NR1C3 | PPARγ | Recettore-γ . attivato dal proliferatore dei perossisomi | PPARGA | |||||
| D | Rev-ErbA | NR1D1 | Rev-ErbAα | Rev-ErbAα | NR1D1 | eme | ||
| NR1D2 | Rev-ErbAβ | Rev-ErbAα | NR1D2 | |||||
| E | E78C-like (artropodi, trematodi, mullosc, nematodi) |
NR1E1 | Eip78C | Proteina 78C . indotta da ecdisone | Eip78C | |||
| F | Recettore orfano correlato a RAR | NR1F1 | RORα | Recettore orfano correlato a RAR-α | RORA | colesterolo , ATRA | ||
| NR1F2 | RORβ | Recettore orfano correlato a RAR-β | RORB | |||||
| NR1F3 | RORγ | Recettore orfano correlato a RAR-γ | RORC | |||||
| G | CNR14-simile (nematode) | NR1G1 | sesso-1 | Recettore dell'ormone steroideo cnr14 | sesso-1 | |||
| h | Recettore X del fegato -simile | NR1H1 | EcR | Recettore dell'ecdisone, EcR (artropodi) | EcR | ecdysteroidi | ||
| NR1H2 | LXRβ | Recettore X del fegato-β | NR1H2 | ossisteroli | ||||
| NR1H3 | LXRα | Recettore X-α . del fegato | NR1H3 | |||||
| NR1H4 | FXR | Recettore farnesoide X | NR1H4 | |||||
| NR1H5 | FXR-β | Recettore farnesoide X-β (pseudogene nell'uomo) |
NR1H5P | |||||
| io | Simile al recettore della vitamina D | NR1I1 | VDR | Recettore della vitamina D | VDR | vitamina D | ||
| NR1I2 | PXR | Recettore del pregnane X | NR1I2 | xenobiotici | ||||
| NR1I3 | MACCHINA | Recettore androstano costitutivo | NR1I3 | androstano | ||||
| J | Hr96-like | NR1J1 | Hr96/ Daf-12 | Recettore dell'ormone nucleare HR96 | Hr96 | colesterolo / acido dafacronico | ||
| NR1J2 | ||||||||
| NR1J3 | ||||||||
| K | Hr1-like | NR1K1 | Hr1 | Recettore dell'ormone nucleare HR1 | ||||
| 2 | Simile al recettore del retinoide X | UN | Fattore nucleare degli epatociti-4 | NR2A1 | HNF4α | Fattore nucleare degli epatociti-4-α | HNF4A | acidi grassi |
| NR2A2 | HNF4γ | Fattore nucleare degli epatociti-4-γ | HNF4G | |||||
| B | Recettore del retinoide X | NR2B1 | RXRα | Recettore del retinoide X-α | RXRA | retinoidi | ||
| NR2B2 | RXRβ | Recettore del retinoide X-β | RXRB | |||||
| NR2B3 | RXRγ | Recettore del retinoide X-γ | RXRG | |||||
| NR2B4 | USP | Proteina dell'ultraspiracolo (artropodi) | usp | fosfolipidi | ||||
| C | Recettore testicolare | NR2C1 | TR2 | Recettore testicolare 2 | NR2C1 | |||
| NR2C2 | TR4 | Recettore testicolare 4 | NR2C2 | |||||
| E | TLX/PNR | NR2E1 | TLX | Omologo del gene senza coda della Drosophila | NR2E1 | |||
| NR2E3 | PNR | Recettore nucleare specifico delle cellule dei fotorecettori | NR2E3 | |||||
| F | COUP /EAR | NR2F1 | COUP-TFI | Fattore di trascrizione promotore a monte dell'ovoalbumina di pollo I | NR2F1 | |||
| NR2F2 | COUP-TFII | Fattore di trascrizione promotore a monte dell'ovoalbumina di pollo II | NR2F2 | acido retinoico (debole) | ||||
| NR2F6 | EAR-2 | Relativo a V-erbA | NR2F6 | |||||
| 3 | Simile al recettore degli estrogeni | UN | Recettore degli estrogeni | NR3A1 | ERα | Recettore degli estrogeni-α | ESR1 | estrogeni |
| NR3A2 | ERβ | Recettore degli estrogeni-β | VES2 | |||||
| B | Recettore correlato agli estrogeni | NR3B1 | ERRα | Recettore correlato agli estrogeni-α | ESRR | |||
| NR3B2 | ERRβ | Recettore correlato agli estrogeni-β | ESRRB | |||||
| NR3B3 | ERRγ | Recettore correlato agli estrogeni-γ | ESRRG | |||||
| C | Recettori 3-chetosteroidi | NR3C1 | GR | Recettore glucocorticoide | NR3C1 | cortisolo | ||
| NR3C2 | SIG | Recettore mineralcorticoide | NR3C2 | aldosterone | ||||
| NR3C3 | PR | Recettore del progesterone | PGR | progesterone | ||||
| NR3C4 | AR | Recettore degli androgeni | AR | testosterone | ||||
| D | Simil -recettore degli estrogeni (nei lofotrocozoi ) |
NR3D | ||||||
| E | Simil-recettore degli estrogeni (negli cnidari ) |
NR3E | ||||||
| F | Simil -recettore degli estrogeni (nei placozoi ) |
NR3F | ||||||
| 4 | Fattore di crescita nervoso simile a IB | UN | NGFIB/NURR1/NOR1 | NR4A1 | NGFIB | Nerve Fattore di crescita IB | NR4A1 | |
| NR4A2 | NURR1 | 1 . correlato al recettore nucleare | NR4A2 | |||||
| NR4A3 | NOR1 | Recettore orfano 1 . derivato dal neurone | NR4A3 | |||||
| 5 | Simil -fattore steroideo |
UN | SF1/LRH1 | NR5A1 | SF1 | Fattore steroideo 1 | NR5A1 | fosfatidilinositolo |
| NR5A2 | LRH-1 | Recettore epatico omologo-1 | NR5A2 | fosfatidilinositolo | ||||
| B | Hr39-like | NR5B1 | HR39/ FTZ-F1 | Recettore dell'ormone nucleare fushi tarazu fattore I beta | Hr39 | |||
| 6 | Cellula germinale simile al fattore nucleare | UN | GCNF | NR6A1 | GCNF | Fattore nucleare delle cellule germinali | NR6A1 | |
| 7 | NR con due domini di legame al DNA (vermi piatti, molluschi, artropodi) |
UN | 2DBD-NRα | NR7A1 | ||||
| B | 2DBD-NRβ | NR7B1 | ||||||
| C | 2DBD-NRγ | NR7C1 | artropodi "α/β" | |||||
| 8 | NR8 ( eumetazoi ) | UN | NR8A | NR8A1 | CgNR8A1 | Recettore nucleare 8 | AKG49571 | |
| 0 | Varie (manca LBD o DBD) | UN | knr/knrl/egon (artropodi) | NR0A1 | KNI | Knirps proteici con gap zigotico | knl | |
| B | DAX/SHP | NR0B1 | DAX1 | Inversione del sesso sensibile al dosaggio, regione critica dell'ipoplasia surrenalica, sul cromosoma X, gene 1 | NR0B1 | |||
| NR0B2 | SHP | Piccolo partner eterodimero | NR0B2 | |||||
Delle due famiglie 0, 0A ha un DBD simile alla famiglia 1 e 0B ha un LBD davvero unico. Il secondo DBD della famiglia 7 è probabilmente correlato alla famiglia 1 DBD. Tre probabilmente NR di famiglia 1 da Biomphalaria glabrata possiedono un DBD insieme a un LBD simile alla famiglia 0B. Il posizionamento di C. elegans nhr-1 ( Q21878 ) è controverso: sebbene la maggior parte delle fonti lo collochi come NR1K1, l'annotazione manuale su WormBase lo considera un membro di NR2A. C'era un gruppo 2D per il quale l'unico membro era Drosophilia HR78/NR1D1 ( Q24142 ) e ortologhi, ma è stato fuso nel gruppo 2C in seguito a causa dell'elevata somiglianza, formando un "gruppo 2C/D". Studi knockout su topi e moscerini della frutta supportano tale gruppo unito.
Evoluzione
Un argomento di dibattito è stato l'identità del recettore nucleare ancestrale come recettore orfano o legante ligando . Questo dibattito è iniziato più di venticinque anni fa, quando i primi ligandi sono stati identificati come steroidi di mammifero e ormoni tiroidei. Poco dopo, l'identificazione del recettore dell'ecdisone in Drosophila ha introdotto l'idea che i recettori nucleari fossero recettori ormonali che legano i ligandi con un'affinità nanomolare. All'epoca, i tre ligandi dei recettori nucleari conosciuti erano steroidi, retinoidi e ormone tiroideo, e di questi tre, sia gli steroidi che i retinoidi erano prodotti del metabolismo dei terpenoidi. Pertanto, è stato postulato che il recettore ancestrale sarebbe stato legato da una molecola terpenoide.
Nel 1992, un confronto del dominio di legame al DNA di tutti i recettori nucleari conosciuti ha portato alla costruzione di un albero filogenico del recettore nucleare che indicava che tutti i recettori nucleari condividevano un antenato comune. Di conseguenza, c'è stato un maggiore sforzo per scoprire lo stato del primo recettore nucleare, e nel 1997 è stata suggerita un'ipotesi alternativa: il recettore nucleare ancestrale era un recettore orfano e ha acquisito la capacità di legare il ligando nel tempo Questa ipotesi è stata proposta sulla base sui seguenti argomenti:
- Le sequenze dei recettori nucleari che erano state identificate nei primi metazoi (cnidari e Schistosoma ) erano tutti membri dei gruppi di recettori COUP-TF, RXR e FTZ-F1. Sia COUP-TF che FTZ-F1 sono recettori orfani e si è scoperto che RXR lega un ligando solo nei vertebrati.
- Mentre i recettori orfani conoscevano gli omologhi degli artropodi, non erano stati identificati ortologhi dei recettori dei vertebrati con legatura al di fuori dei vertebrati, suggerendo che i recettori orfani sono più vecchi dei recettori con legatura.
- I recettori orfani si trovano tra tutte e sei le sottofamiglie di recettori nucleari, mentre i recettori dipendenti dal ligando si trovano tra tre. Pertanto, poiché si riteneva che i recettori dipendenti dal ligando fossero prevalentemente membri di sottofamiglie recenti, sembrava logico che acquisissero la capacità di legare i ligandi in modo indipendente.
- La posizione filogenetica di un dato recettore nucleare all'interno dell'albero è correlata al suo dominio di legame al DNA e alle capacità di dimerizzazione, ma non esiste una relazione identificata tra un recettore nucleare ligando-dipendente e la natura chimica del suo ligando. Oltre a ciò, le relazioni evolutive tra i recettori ligando-dipendenti non avevano molto senso in quanto recettori strettamente correlati di ligandi legati a sottofamiglie provenienti da percorsi biosintetici completamente diversi (es. TR e RAR). D'altra parte, le sottofamiglie che non sono correlate evolutivamente legano ligandi simili (RAR e RXR legano entrambi rispettivamente l'acido all-trans e 9-cis retinoico).
- Nel 1997 si scoprì che non esistevano recettori nucleari in conformazioni statiche off e on, ma che un ligando poteva alterare l'equilibrio tra i due stati. Inoltre, è stato scoperto che i recettori nucleari potrebbero essere regolati in modo indipendente dal ligando, attraverso la fosforilazione o altre modificazioni post-traduzionali. Pertanto, questo ha fornito un meccanismo per il modo in cui un recettore orfano ancestrale è stato regolato in modo indipendente dal ligando e ha spiegato perché il dominio di legame del ligando è stato conservato.
Nel corso dei successivi 10 anni, furono condotti esperimenti per testare questa ipotesi e presto emersero controargomentazioni:
- I recettori nucleari sono stati identificati nel genoma appena sequenziato del demosponge Amphimedon queenslandica , un membro Porifera, il più antico phylum di metazoi. Il genoma di A. queenslandica contiene due recettori nucleari noti come AqNR1 e AqNR2 ed entrambi sono stati caratterizzati per legarsi ed essere regolati da ligandi.
- Sono stati trovati omologhi per i recettori vertebrati dipendenti dal ligando al di fuori dei vertebrati nei molluschi e nei platelminti. Inoltre, è stato scoperto che i recettori nucleari trovati negli cnidari hanno ligandi strutturali nei mammiferi, che potrebbero rispecchiare la situazione ancestrale.
- Due presunti recettori orfani , HNF4 e USP, sono stati trovati, tramite analisi strutturale e di spettrometria di massa, per legare rispettivamente acidi grassi e fosfolipidi.
- I recettori nucleari e i ligandi risultano essere molto meno specifici di quanto si pensasse in precedenza. I retinoidi possono legare recettori di mammifero diversi da RAR e RXR come PPAR, RORb o COUP-TFII. Inoltre, RXR è sensibile a un'ampia gamma di molecole tra cui retinoidi, acidi grassi e fosfolipidi.
- Lo studio dell'evoluzione del recettore degli steroidi ha rivelato che il recettore ancestrale degli steroidi potrebbe legare un ligando, l'estradiolo. Al contrario, il recettore degli estrogeni trovato nei molluschi è costitutivamente attivo e non si lega agli ormoni correlati agli estrogeni. Quindi, questo ha fornito un esempio di come un recettore ancestrale dipendente dal ligando potrebbe perdere la sua capacità di legare i ligandi.
Una combinazione di queste recenti prove, nonché uno studio approfondito della struttura fisica del dominio di legame del ligando del recettore nucleare ha portato all'emergere di una nuova ipotesi sullo stato ancestrale del recettore nucleare. Questa ipotesi suggerisce che il recettore ancestrale possa agire come un sensore lipidico con la capacità di legare, anche se piuttosto debolmente, diverse molecole idrofobiche come retinoidi, steroidi, emi e acidi grassi. Con la sua capacità di interagire con una varietà di composti, questo recettore, attraverso duplicazioni, perderebbe la sua capacità di attività ligando-dipendente o si specializzerebbe in un recettore altamente specifico per una particolare molecola.
Storia
Di seguito è riportata una breve selezione di eventi chiave nella storia della ricerca sui recettori nucleari.
- 1905 – Ernest Starling conia la parola ormone
- 1926 – Edward Calvin Kendall e Tadeus Reichstein isolano e determinano le strutture del cortisone e della tiroxina
- 1929 – Adolf Butenandt e Edward Adelbert Doisy – isolarono indipendentemente e determinarono la struttura dell'estrogeno
- 1958 – Elwood Jensen – isolò il recettore degli estrogeni
- 1980 - clonazione del estrogeni, glucocorticoidi, e recettore degli ormoni tiroidei da Pierre Chambon , Ronald Evans , e Björn Vennström rispettivamente
- 2004 – Pierre Chambon, Ronald Evans ed Elwood Jensen hanno ricevuto l' Albert Lasker Award per la ricerca medica di base , un premio che spesso precede un premio Nobel per la medicina
Guarda anche
Riferimenti
link esterno
- Nucleare+Recettori presso la Biblioteca Nazionale di Medicina degli Stati Uniti Medical Subject Headings (MeSH)
- Vincent Laudet (2006). "The IUPHAR Compendium of the Pharmacology and Classification of the Nuclear Receptor Superfamily 2006E" . Compendio sui recettori nucleari . L'Unione Internazionale di Farmacologia di Base e Clinica . Estratto il 21/02/2008 .
- " Rivista online sui recettori nucleari " . Pagina iniziale . pubblicato da BioMed Central (non accetta più contributi da maggio 2007) . Estratto il 21/02/2008 .
- "Risorsa del recettore nucleare" . Università di Georgetown. Archiviato dall'originale il 2008-05-11 . Estratto il 21/02/2008 .
-
"Atlante di segnalazione dei recettori nucleari (recettori, coattivatori, corepressori e ligandi)" . Il Consorzio NURSA . Estratto il 21/02/2008 .
un consorzio di ricerca e un database finanziati dal NIH; include una rivista indicizzata su PubMed ad accesso aperto, Nuclear Receptor Signaling
- "Risorsa del recettore nucleare" . Jack Vanden Heuvel . Estratto 2009-09-21 .