Fenilchetonuria - Phenylketonuria
| Fenilchetonuria | |
|---|---|
| Altri nomi | Deficit di fenilalanina idrossilasi, deficit di PAH, malattia di Følling |
 | |
| fenilalanina | |
| Specialità | Genetica medica , pediatria |
| Sintomi | Senza trattamento disabilità intellettiva , convulsioni , problemi comportamentali, disturbi mentali , odore di muffa |
| Esordio normale | Alla nascita |
| tipi | Classico, variante |
| cause | Genetico ( autosomico recessivo ) |
| Metodo diagnostico | Programmi di screening neonatale in molti paesi |
| Trattamento | Dieta a basso contenuto di alimenti che contengono fenilalanina; integratori speciali |
| Farmaco | Sapropterina dicloridrato , pegvaliasi |
| Prognosi | Salute normale con il trattamento |
| Frequenza | ~1 su 12.000 neonati |
Fenilchetonuria ( PKU ) è un difetto congenito del metabolismo che si traduce in diminuzione del metabolismo del aminoacido fenilalanina . Non trattata, la PKU può portare a disabilità intellettiva , convulsioni , problemi comportamentali e disturbi mentali . Può anche provocare un odore di muffa e una pelle più chiara. Un bambino nato da una madre che ha una PKU mal trattata può avere problemi cardiaci, testa piccola e basso peso alla nascita .
La fenilchetonuria è una malattia genetica ereditata dai genitori di una persona. È dovuto a mutazioni nel gene PAH , che si traduce in bassi livelli dell'enzima fenilalanina idrossilasi . Ciò si traduce nell'accumulo di fenilalanina nella dieta a livelli potenzialmente tossici. È autosomica recessiva , il che significa che entrambe le copie del gene devono essere mutate affinché la condizione si sviluppi. Esistono due tipi principali, la PKU classica e la PKU variante, a seconda che rimanga una funzione enzimatica. Quelli con una copia di un gene mutato in genere non hanno sintomi. Molti paesi hanno programmi di screening neonatale per la malattia.
Il trattamento è con una dieta che (1) è a basso contenuto di alimenti che contengono fenilalanina e che (2) include integratori speciali. I bambini dovrebbero usare una formula speciale con una piccola quantità di latte materno . La dieta dovrebbe iniziare il prima possibile dopo la nascita e continuare per tutta la vita. Le persone che ricevono una diagnosi precoce e seguono una dieta rigorosa possono avere una salute normale e una durata di vita normale . L'efficacia viene monitorata attraverso esami del sangue periodici. Il farmaco sapropterina dicloridrato può essere utile in alcuni.
La fenilchetonuria colpisce circa 1 bambino su 12.000. Maschi e femmine sono colpiti allo stesso modo. La malattia è stata scoperta nel 1934 da Ivar Asbjørn Følling , con l'importanza della dieta determinata nel 1953. La terapia genica , sebbene promettente, richiede molti più studi a partire dal 2014.
segni e sintomi
La PKU non trattata può portare a disabilità intellettiva , convulsioni , problemi comportamentali e disturbi mentali . Può anche provocare un odore di muffa e una pelle più chiara. Un bambino nato da una madre che ha una PKU mal trattata può avere problemi cardiaci, testa piccola e basso peso alla nascita .
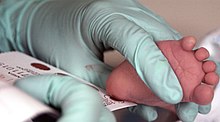
Poiché il corpo della madre è in grado di scomporre la fenilalanina durante la gravidanza, i bambini con PKU sono normali alla nascita. La malattia non è rilevabile all'esame obiettivo in quel momento, perché nessun danno è stato ancora fatto. Lo screening neonatale viene eseguito per rilevare la malattia e iniziare il trattamento prima che si verifichi qualsiasi danno. Il campione di sangue viene solitamente prelevato da una puntura del tallone , in genere eseguita 2-7 giorni dopo la nascita. Questo test può rivelare livelli di fenilalanina elevati dopo uno o due giorni di normale alimentazione del bambino.
Se un bambino non viene diagnosticato durante il test di screening neonatale di routine e non viene introdotta una dieta a ridotto contenuto di fenilalanina, i livelli di fenilalanina nel sangue aumenteranno nel tempo. Livelli tossici di fenilalanina (e livelli insufficienti di tirosina) possono interferire con lo sviluppo infantile in modi che hanno effetti permanenti. La malattia può presentarsi clinicamente con convulsioni , ipopigmentazione (capelli e pelle eccessivamente chiari) e un "odore di muffa" nel sudore e nelle urine del bambino (dovuto al fenilacetato , un acido carbossilico prodotto dall'ossidazione del fenilchetone). Nella maggior parte dei casi, è necessario ripetere il test a circa due settimane di età per verificare il test iniziale e scoprire l'eventuale fenilchetonuria inizialmente mancata.
I bambini non trattati spesso non riescono a raggiungere le prime tappe dello sviluppo, sviluppano la microcefalia e dimostrano una progressiva compromissione della funzione cerebrale. L'iperattività , le anomalie dell'EEG , le convulsioni e le gravi difficoltà di apprendimento sono i principali problemi clinici più avanti nella vita. Un caratteristico odore "di muffa o di topo" sulla pelle, nonché una predisposizione all'eczema , persistono per tutta la vita in assenza di trattamento.
Il danno arrecato al cervello se la PKU non viene trattata durante i primi mesi di vita non è reversibile. È fondamentale controllare la dieta dei neonati con PKU con molta attenzione in modo che il cervello abbia l'opportunità di svilupparsi normalmente. I bambini affetti che vengono rilevati alla nascita e trattati hanno molte meno probabilità di sviluppare problemi neurologici o avere convulsioni e disabilità intellettiva (sebbene tali disturbi clinici siano ancora possibili tra cui asma, eczema, anemia, aumento di peso, insufficienza renale, osteoporosi, gastrite, esofago e carenze renali, calcoli renali e ipertensione). Inoltre, i disturbi depressivi maggiori si verificano il 230% in più rispetto ai controlli; vertigini e vertigini si verificano il 180% in più; cardiopatia ischemica cronica, asma, diabete e gastroenterite si verificano più del 170%; e i disturbi da stress e adattamento si verificano il 160% in più. In generale, tuttavia, i risultati per le persone trattate per PKU sono buoni. Le persone trattate potrebbero non avere alcun problema fisico, neurologico o di sviluppo rilevabile.
Genetica

PKU è un autosomica recessiva metabolica malattia genetica . Essendo una malattia autosomica recessiva, sono necessari due alleli PKU affinché un individuo manifesti i sintomi della malattia. Affinché un bambino erediti la PKU, sia la madre che il padre devono avere e trasmettere il gene difettoso. Se entrambi i genitori sono portatori di PKU, c'è una probabilità del 25% che un bambino che hanno nasca con il disturbo, una probabilità del 50% che il bambino sia un portatore e una probabilità del 25% che il bambino non si sviluppi né sia un portatore per la malattia.
La PKU è caratterizzata da mutazioni omozigoti o eterozigoti composte nel gene per l'enzima epatico fenilalanina idrossilasi (PAH), che lo rendono non funzionale. Questo enzima è necessario per metabolizzare l'aminoacido fenilalanina (Phe) nell'aminoacido tirosina (Tyr). Quando l'attività della PAH è ridotta, la fenilalanina si accumula e viene convertita in fenilpiruvato (noto anche come fenilchetone), che può essere rilevato nelle urine .
Portatori di un singolo allele PKU non presentano sintomi della malattia, ma sembrano essere protetti in una certa misura contro tossina fungina ocratossina A . Ciò spiega la persistenza dell'allele in alcune popolazioni in quanto conferisce un vantaggio selettivo, in altre parole, essere un eterozigote è vantaggioso .
Il gene PAH si trova sul cromosoma 12 nelle bande 12q22-q24.2. A partire dal 2000, erano state trovate circa 400 mutazioni patogenetiche nel gene PAH. Questo è un esempio di eterogeneità genetica allelica .
Fisiopatologia
Quando la fenilalanina (Phe) non può essere metabolizzata dall'organismo, una dieta tipica che sarebbe salutare per le persone senza PKU provoca l'accumulo di livelli anormalmente elevati di Phe nel sangue, che è tossico per il cervello. Se non trattata (e spesso anche in trattamento), le complicanze della PKU includono grave disabilità intellettiva, anomalie della funzione cerebrale, microcefalia, disturbi dell'umore, funzionamento motorio irregolare e problemi comportamentali come il disturbo da deficit di attenzione e iperattività , nonché sintomi fisici come un odore "di muffa", eczema e colorazione della pelle e dei capelli insolitamente chiara.
PKU classico
La PKU classica e le sue forme meno gravi "PKU lieve" e "iperfenilalaninemia lieve" sono causate da un gene mutato per l' enzima fenilalanina idrossilasi (PAH), che converte l'aminoacido fenilalanina ("Phe") in altri composti essenziali nel corpo , in particolare tirosina. La tirosina è un amminoacido condizionatamente essenziale per i pazienti con PKU perché senza PAH non può essere prodotta nel corpo attraverso la scomposizione della fenilalanina. La tirosina è necessaria per la produzione di neurotrasmettitori come l'adrenalina, la noradrenalina e la dopamina.
Il deficit di PAH provoca uno spettro di disturbi, tra cui la fenilchetonuria classica (PKU) e la lieve iperfenilalaninemia (nota anche come "iperfe" o "lieve HPA"), un accumulo meno grave di fenilalanina. Rispetto ai pazienti con PKU classica, i pazienti con "iperfe" hanno una maggiore attività enzimatica della PAH e sono in grado di tollerare maggiori quantità di fenilalanina nella loro dieta. Senza un intervento dietetico, i pazienti con HPA lieve hanno livelli di Phe nel sangue più alti di quelli con normale attività di PAH. Attualmente non esiste un consenso internazionale sulla definizione di HPA lieve, tuttavia è più frequentemente diagnosticata a livelli di Phe nel sangue compresi tra 2-6 mg/dL.
La fenilalanina è un grande amminoacido neutro (LNAA). Gli LNAA competono per il trasporto attraverso la barriera emato-encefalica (BBB) attraverso il grande trasportatore di aminoacidi neutri (LNAAT). Se la fenilalanina è in eccesso nel sangue, saturerà il trasportatore. Livelli eccessivi di fenilalanina tendono a diminuire i livelli di altri LNAA nel cervello. Poiché questi amminoacidi sono necessari per la sintesi di proteine e neurotrasmettitori, l'accumulo di Phe ostacola lo sviluppo del cervello , causando disabilità intellettiva .
Ricerche recenti suggeriscono che neurocognitivo, psicosociale, qualità della vita, crescita, nutrizione, patologia ossea sono leggermente subottimali anche per i pazienti che vengono trattati e mantengono i loro livelli di Phe nell'intervallo target, se la loro dieta non è integrata con altri aminoacidi.
La PKU classica colpisce la mielinizzazione e i tratti della sostanza bianca nei neonati non trattati; questa può essere una delle principali cause di problemi neurologici associati alla fenilchetonuria. Le differenze nello sviluppo della sostanza bianca sono osservabili con la risonanza magnetica . Possono essere rilevate anche anomalie nella sostanza grigia, in particolare nella corteccia motoria e premotoria, nel talamo e nell'ippocampo.
È stato recentemente suggerito che la PKU possa assomigliare alle malattie amiloidi , come il morbo di Alzheimer e il morbo di Parkinson, a causa della formazione di aggregati tossici di fenilalanina simili all'amiloide.
Anche altre mutazioni non PAH possono causare PKU.
Iperfenilalaninemia da deficit di tetraidrobiopterina
Una forma più rara di iperfenilalaninemia è il deficit di tetraidrobiopterina , che si verifica quando l'enzima PAH è normale e si riscontra un difetto nella biosintesi o nel riciclaggio del cofattore tetraidrobiopterina (BH 4 ). BH 4 è necessario per la corretta attività dell'enzima PAH e questo coenzima può essere integrato come trattamento. Coloro che soffrono di questa forma di iperfenilalaninemia possono avere una carenza di tirosina (che viene creata dalla fenilalanina dalla PAH), nel qual caso il trattamento è l'integrazione di tirosina per spiegare questa carenza.
I livelli di dopamina possono essere utilizzati per distinguere tra questi due tipi. La tetraidrobiopterina è necessaria per convertire Phe in Tyr ed è necessaria per convertire Tyr in L-DOPA tramite l'enzima tirosina idrossilasi . La L-DOPA, a sua volta, viene convertita in dopamina . Bassi livelli di dopamina portano ad alti livelli di prolattina . Al contrario, nella PKU classica (senza coinvolgimento di diidrobiopterina), i livelli di prolattina sarebbero relativamente normali.
La carenza di tetraidrobiopterina può essere causata da difetti in quattro geni. Sono conosciuti come HPABH4A, HPABH4B, HPABH4C e HPABH4D.
Percorsi metabolici

L'enzima fenilalanina idrossilasi converte normalmente l' aminoacido fenilalanina nell'aminoacido tirosina . Se questa reazione non avviene, la fenilalanina si accumula e la tirosina è carente. L'eccessiva fenilalanina può essere metabolizzata in fenilchetoni attraverso la via minore, una via delle transaminasi con il glutammato . I metaboliti includono fenilacetato , fenilpiruvato e fenetilammina . Elevati livelli di fenilalanina nel sangue e il rilevamento di fenilchetoni nelle urine sono diagnostici, tuttavia la maggior parte dei pazienti viene diagnosticata tramite screening neonatale.
Selezione
La PKU è comunemente inclusa nel pannello di screening neonatale di molti paesi, con varie tecniche di rilevamento. La maggior parte dei bambini nei paesi sviluppati viene sottoposta a screening per la PKU subito dopo la nascita. Lo screening per la PKU viene eseguito con test di inibizione batterica ( test di Guthrie ), test immunologici mediante rilevamento fluorometrico o fotometrico o misurazione degli amminoacidi mediante spettrometria di massa tandem (MS/MS). Le misurazioni effettuate utilizzando MS/MS determinano la concentrazione di Phe e il rapporto tra Phe e tirosina , il rapporto sarà elevato nella PKU.
Trattamento
PKU non è curabile. Tuttavia, se la PKU viene diagnosticata abbastanza presto, un neonato affetto può crescere con un normale sviluppo cerebrale gestendo e controllando i livelli di fenilalanina ("Phe") attraverso la dieta o una combinazione di dieta e farmaci.
Dieta
Le persone che seguono il trattamento dietetico prescritto dalla nascita possono (ma non sempre) non avere sintomi. La loro PKU sarebbe rilevabile solo con un esame del sangue. Le persone devono seguire una dieta speciale a basso contenuto di Phe per uno sviluppo ottimale del cervello. Poiché il Phe è necessario per la sintesi di molte proteine, è necessario per una crescita appropriata, ma i livelli devono essere rigorosamente controllati.
Per le persone che non hanno fenilchetonuria, il set dell'Istituto di Medicina degli Stati Uniti ha raccomandato almeno 33 mg/kg di peso corporeo/giorno di fenilalanina più tirosina per gli adulti di età pari o superiore a 19 anni. Per le persone con PKU, una raccomandazione per i bambini fino a 10 anni è di 200-500 mg/die; per i bambini più grandi e gli adulti al di sotto di 600 mg/die. Dove nell'intervallo dipende dal peso corporeo, dall'età e dal monitoraggio della concentrazione ematica.
Gli intervalli di salute ottimali (o "intervalli target") sono compresi tra 120 e 360 μmol/L o equivalentemente da 2 a 6 mg/dL. Questo deve essere raggiunto in modo ottimale durante almeno i primi 10 anni, per consentire al cervello di svilupparsi normalmente.
La dieta richiede di limitare o eliminare cibi ricchi di Phe, come soia , albume d'uovo , gamberi , petto di pollo , spirulina , crescione , pesce , noci , gamberi di fiume , aragosta , tonno , tacchino , legumi e ricotta a basso contenuto di grassi . I cibi ricchi di amido, come patate e mais, sono generalmente accettabili in quantità controllate, ma la quantità di Phe consumata da questi alimenti deve essere monitorata. In alcuni casi può essere prescritta una dieta priva di mais. Di solito viene tenuto un diario alimentare per registrare la quantità di Phe consumata con ogni pasto, spuntino o bevanda. Un sistema di "scambio" può essere utilizzato per calcolare la quantità di Phe in un alimento dal contenuto proteico identificato su un'etichetta informativa nutrizionale. I sostituti del "cibo medico" a basso contenuto proteico vengono spesso utilizzati al posto del normale pane , pasta e altri alimenti a base di cereali, che contengono una quantità significativa di Phe. Molti frutti e verdure sono più bassi di Phe e possono essere consumati in quantità maggiori. I neonati possono ancora essere allattati al seno per fornire tutti i benefici del latte materno, ma anche la quantità deve essere monitorata e sarà necessaria l'integrazione per i nutrienti mancanti. Da evitare anche il dolcificante aspartame , presente in molti alimenti dietetici e bibite analcoliche, in quanto l'aspartame contiene fenilalanina.
Persone diverse possono tollerare quantità diverse di Phe nella loro dieta. Gli esami del sangue regolari vengono utilizzati per determinare gli effetti dell'assunzione di Phe nella dieta sul livello di Phe nel sangue.
Supplementi nutrizionali
Le formule supplementari di "sostituto proteico" sono tipicamente prescritte per le persone con PKU (a partire dall'infanzia) per fornire gli amminoacidi e altri nutrienti necessari che altrimenti mancherebbero in una dieta a basso contenuto di fenilalanina. La tirosina, che normalmente è derivata dalla fenilalanina e che è necessaria per la normale funzione cerebrale, è solitamente integrata. Il consumo delle formule sostitutive proteiche può effettivamente ridurre i livelli di fenilalanina, probabilmente perché impedisce al processo di catabolismo proteico di rilasciare Phe immagazzinato nei muscoli e in altri tessuti nel sangue. Molti pazienti con PKU hanno i livelli più alti di Phe dopo un periodo di digiuno (come la notte), perché il digiuno innesca il catabolismo. Una dieta povera di fenilalanina ma che non include sostituti proteici può anche non riuscire ad abbassare i livelli di Phe nel sangue, poiché una dieta nutrizionalmente insufficiente può anche innescare il catabolismo. Per tutti questi motivi, la formula di prescrizione è una parte importante del trattamento per i pazienti con PKU classica.
Le prove supportano l'integrazione alimentare con grandi amminoacidi neutri (LNAA). Gli LNAA (es. leu , tyr , trp , met , his , ile , val , thr ) possono competere con phe per specifiche proteine di trasporto che trasportano gli LNAA attraverso la mucosa intestinale nel sangue e attraverso la barriera ematoencefalica nel cervello. Il suo uso è limitato negli Stati Uniti a causa del costo, ma è disponibile nella maggior parte dei paesi come parte di una dieta a basso contenuto proteico / PHE per sostituire i nutrienti mancanti.
Un'altra strategia di trattamento interessante è il glicomacropeptide della caseina (CGMP), che è un peptide del latte naturalmente privo di Phe nella sua forma pura CGMP può sostituire la maggior parte degli aminoacidi liberi nella dieta PKU e fornisce diversi effetti nutrizionali benefici rispetto agli aminoacidi liberi acidi. Il fatto che il CGMP sia un peptide assicura che il tasso di assorbimento dei suoi amminoacidi sia prolungato rispetto agli amminoacidi liberi e quindi si traduce in una migliore ritenzione proteica e un aumento della sazietà rispetto agli amminoacidi liberi. Un altro importante vantaggio del CGMP è che il gusto è significativamente migliorato quando il CGMP sostituisce parte degli amminoacidi liberi e questo può aiutare a garantire una migliore compliance alla dieta PKU.
Inoltre, il CGMP contiene un'elevata quantità di LNAA che riducono il phe, che costituisce circa 41 g per 100 g di proteine e quindi aiuterà a mantenere i livelli plasmatici di phe nell'intervallo target.
Sostituti enzimatici
Nel 2018, la FDA ha approvato un sostituto enzimatico chiamato pegvaliase che metabolizza la fenilalanina. È per gli adulti che sono mal gestiti su altri trattamenti.
La tetraidrobiopterina (BH4) (un cofattore per l' ossidazione della fenilalanina) se assunta per via orale può ridurre i livelli ematici di questo amminoacido in alcune persone.
Madri
Per le donne con PKU, è importante per la salute dei loro figli mantenere bassi livelli di Phe prima e durante la gravidanza. Sebbene il feto in via di sviluppo possa essere solo un portatore del gene PKU, l'ambiente intrauterino può avere livelli molto elevati di fenilalanina, che può attraversare la placenta. Il bambino può sviluppare malattie cardiache congenite, ritardo della crescita, microcefalia e disabilità intellettiva. Le stesse donne affette da PKU non sono a rischio di ulteriori complicazioni durante la gravidanza.
Nella maggior parte dei paesi, si consiglia alle donne con PKU che desiderano avere figli di abbassare i livelli di Phe nel sangue (in genere tra 2 e 6 mg/dL) prima di iniziare una gravidanza e di controllare attentamente i loro livelli durante la gravidanza. Ciò si ottiene eseguendo regolari esami del sangue e attenendosi molto rigorosamente a una dieta, in genere monitorata quotidianamente da un dietologo metabolico specializzato. In molti casi, quando il fegato del feto inizia a svilupparsi e a produrre normalmente PAH, i livelli di Phe nel sangue della madre diminuiranno, richiedendo una maggiore assunzione per rimanere nell'intervallo di sicurezza di 2-6 mg/dL. Di conseguenza, l'assunzione giornaliera di Phe della madre può raddoppiare o addirittura triplicare entro la fine della gravidanza. Quando i livelli di Phe nel sangue materno scendono al di sotto di 2 mg/dL, i rapporti aneddotici indicano che le madri possono subire effetti avversi, tra cui mal di testa, nausea, perdita di capelli e malessere generale. Quando vengono mantenuti bassi livelli di fenilalanina per tutta la durata della gravidanza, non ci sono livelli elevati di rischio di difetti alla nascita rispetto a un bambino nato da madre non PKU.
Epidemiologia
| Nazione | Incidenza |
|---|---|
| Australia | 1 su 10.000 |
| Brasile | 1 su 8.690 |
| Canada | 1 su 22.000 |
| Cina | 1 su 17.000 |
| Cecoslovacchia | 1 su 7.000 |
| Danimarca | 1 su 12.000 |
| Finlandia | 1 su 200.000 |
| Francia | 1 su 13.500 |
| India | 1 su 18.300 |
| Irlanda | 1 su 4.500 |
| Italia | 1 su 17.000 |
| Giappone | 1 su 125.000 |
| Corea | 1 su 41.000 |
| Olanda | 1 su 18.000 |
| Norvegia | 1 su 14.500 |
| Filippine | 1 su 102.000 |
| Polonia | 1 su 8.000 |
| Scozia | 1 su 5.300 |
| Spagna | 1 su 20.000 |
| Svezia | 1 su 20.000 |
| tacchino | 1 su 2.600 |
| Regno Unito | 1 su 10.000 |
| stati Uniti | 1 su 25.000 |
Il numero medio di nuovi casi di PKU varia nelle diverse popolazioni umane. I caucasici degli Stati Uniti sono colpiti a un tasso di 1 su 10.000. La Turchia ha il più alto tasso documentato al mondo, con 1 su 2.600 nascite, mentre paesi come Finlandia e Giappone hanno tassi estremamente bassi con meno di un caso di PKU su 100.000 nascite. Uno studio del 1987 in Slovacchia riporta una popolazione Rom con un'incidenza estremamente elevata di PKU (un caso su 40 nascite) a causa di un'estesa consanguineità. È il problema metabolico degli aminoacidi più comune nel Regno Unito.
Storia
Prima che le cause della PKU fossero comprese, la PKU causava una grave disabilità nella maggior parte delle persone che avevano ereditato le mutazioni rilevanti. L'autrice Pearl S. Buck, vincitrice del premio Nobel e Pulitzer, aveva una figlia di nome Carol che viveva con la PKU prima che fosse disponibile il trattamento e ha scritto un resoconto dei suoi effetti in un libro intitolato The Child Who Never Grew. Molti pazienti con PKU non trattati nati prima dello screening neonatale diffuso sono ancora vivi, in gran parte in case/istituzioni di vita dipendenti.
La fenilchetonuria fu scoperta dal medico norvegese Ivar Asbjørn Følling nel 1934 quando notò che l'iperfenilalaninemia (HPA) era associata a disabilità intellettiva. In Norvegia, questo disturbo è noto come malattia di Følling, dal nome del suo scopritore. Følling è stato uno dei primi medici ad applicare analisi chimiche dettagliate allo studio delle malattie.
Nel 1934 al Rikshospitalet , Følling vide una giovane donna di nome Borgny Egeland. Ha avuto due figli, Liv e Dag, che erano normali alla nascita ma che successivamente hanno sviluppato disabilità intellettiva. Quando Dag aveva circa un anno, la madre notò un forte odore nella sua urina. Følling ottenne campioni di urina dai bambini e, dopo molti test, scoprì che la sostanza che causava l'odore nelle urine era l'acido fenilpiruvico. I bambini, concluse, avevano un eccesso di acido fenilpiruvico nelle urine, la condizione che venne chiamata fenilchetonuria (PKU).
La sua attenta analisi delle urine dei due fratelli affetti lo ha portato a chiedere a molti medici vicino a Oslo di testare l'urina di altri pazienti affetti. Ciò ha portato alla scoperta della stessa sostanza che aveva trovato in altri otto pazienti. Ha condotto test e ha trovato reazioni che hanno dato origine a benzaldeide e acido benzoico , che lo hanno portato a concludere che il composto conteneva un anello benzenico . Ulteriori test hanno mostrato che il punto di fusione era lo stesso dell'acido fenilpiruvico , il che indicava che la sostanza era nelle urine.
Nel 1954, Horst Bickel , Evelyn Hickmans e John Gerrard pubblicarono un articolo che descriveva come avevano creato una dieta a basso contenuto di fenilalanina e il paziente si era ripreso. Bickel, Gerrard e Hickmans ricevettero la John Scott Medal nel 1962 per la loro scoperta.
La PKU è stata la prima malattia ad essere diagnosticata di routine attraverso uno screening neonatale diffuso . Robert Guthrie ha introdotto il test di screening neonatale per la PKU nei primi anni '60. Con la consapevolezza che la PKU poteva essere rilevata prima che i sintomi fossero evidenti e il trattamento fosse iniziato, lo screening è stato rapidamente adottato in tutto il mondo. L'Irlanda è stato il primo paese a introdurre un programma di screening nazionale nel febbraio 1966, anche l'Austria ha iniziato le proiezioni nel 1966 e l'Inghilterra nel 1968.
Nel 2017 sono state pubblicate le Linee Guida Europee. Sono stati richiesti dalle organizzazioni di pazienti come la Società europea per la fenilchetonuria e i disturbi alleati trattati come fenilchetonuria . Hanno ricevuto un'accoglienza critica.
Etimologia e pronuncia
La parola fenilchetonuria usa forme combinate di fenile + chetone + -uria ; è pronunciato / ˌ f Ì n aɪ l ˌ k Ì t ə nj ʊər i ə , ˌ f ɛ n -, - n ɪ l -, - n əl -, - t oʊ - / .
Ricerca
Altre terapie sono attualmente allo studio, compresa la terapia genica .
Biomarin sta attualmente conducendo studi clinici per studiare PEG-PAL (PEGylated recombinant phenylalanine ammonia lyase o "PAL") è una terapia di sostituzione enzimatica in cui l'enzima PAH mancante viene sostituito con un enzima analogo che scompone anche il Phe. PEG-PAL è ora in fase di sviluppo clinico 2.
Guarda anche
- Iperfenillanemia
- Lofenalac
- Deficit di tetraidrobiopterina
- Fiori per Algernon , che presenta un personaggio che ha la fenilchetonuria
Riferimenti
link esterno
| Classificazione | |
|---|---|
| Risorse esterne |