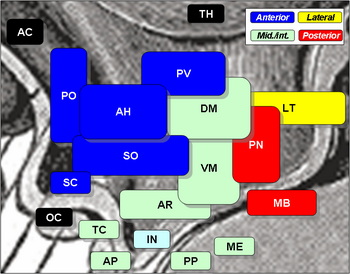
Nucleo preottico mediano - Median preoptic nucleus
| Nucleo preottico mediano | |
|---|---|
| Identificatori | |
| NeuroNames | 378 |
| ID NeuroLex | birnlex_1208 |
| TA98 | A14.1.08.908 |
| TA2 | 5711 |
| FMA | 62323 |
| Termini anatomici di neuroanatomia | |
Il nucleo preoptic mediano si trova dorsale agli altri tre nuclei del preottica della anterior dell'ipotalamo . L'ipotalamo si trova appena sotto il talamo , la principale stazione di trasmissione sensoriale del sistema nervoso , ed è considerato parte del sistema limbico , che comprende anche strutture come l' ippocampo e l' amigdala . L'ipotalamo è altamente coinvolto nel mantenimento dell'omeostasi del corpo e il nucleo preottico mediano non fa eccezione, contribuendo alla regolazione della composizione del sangue, della temperatura corporea e del sonno non REM .
Il nucleo preottico mediano è fortemente coinvolto in tre aree principali. Questi includono l' osmoregolazione , la termoregolazione e l' omeostasi del sonno . All'interno di ogni area sono presenti molte funzioni. Il ruolo che il nucleo preottico mediano gioca nell'osmoregolazione è nella composizione e nel volume del sangue , compreso l'equilibrio dei liquidi e dei sali, e produce risposte che vanno dal comportamentale all'endocrino . La termoregolazione include sia le risposte alle infezioni che alla diminuzione della temperatura interna in seguito all'esposizione cutanea al freddo, entrambe coinvolgono il nucleo preottico mediano come importante mediatore dell'input sensoriale e dell'output regolatorio. L'omeostasi del sonno è coinvolta sia nell'inizio che nel mantenimento del sonno .
Il nucleo preottico mediano ha proiezioni eccitatorie e inibitorie in molte aree del cervello . Ha influenze inibitorie attraverso proiezioni GABAergiche sulle aree del cervello coinvolte nella stimolazione della termogenesi , nonché sulle aree del cervello attive nella veglia per indurre il sonno. La microiniezione di etanolo, triazolam e propofol in quest'area induce il sonno nei roditori, suggerendo che è coinvolto nei loro effetti farmacologici sul sonno. Il glutamatergico e il noradrenergico , così come altri neurotrasmettitori , hanno influenze eccitatorie su altre aree del cervello. Il nucleo preottico mediano è altamente coinvolto nella regolazione cardiovascolare , compreso il rilascio del peptide natriuretico atriale da parte del cuore in risposta all'elevato volume sanguigno . Inoltre, è coinvolto nel controllo della risposta febbrile alle infezioni e nella stimolazione della sete , tra le altre funzioni. Sia la connettività che la posizione anatomica del nucleo preottico mediano gli consentono di essere sia una stazione di trasmissione che un mediatore per le informazioni sensoriali e regolatorie e producono risposte neurali , endocrine e comportamentali per mantenere l' omeostasi .
Posizione
Il nucleo preoptic mediana si trova nella zona preottica del ipotalamo . Formando una parte critica del terzo ventricolo anteroventrale e della linea mediana della lamina terminale , il nucleo preottico mediano occupa una posizione anatomica che gli consente di svolgere un ruolo importante in molti aspetti della regolazione omeostatica . Questa regione è importante per la regolazione cardiovascolare , della pressione sanguigna e della composizione del sangue e riceve input dall'organo subfornicale (SFO) e dall'organo vascolare della lamina terminalis (VOLT), che si trovano al di fuori della barriera ematoencefalica e trasmettono informazioni sull'osmolalità del sangue e livelli di segnali endocrini come il peptide natriuretico atriale (ANP).
Connettività
La connettività con altre regioni dell'ipotalamo , come l' area preottica ventrolaterale (VLPO) e con le regioni del tronco cerebrale, consente anche al nucleo preottico mediano di essere coinvolto in altri aspetti dell'omeostasi . Questi includono comportamenti sonno-veglia, sete e comportamento alcolico, nonché la termoregolazione . Vie parallele nell'area preottica sono coinvolte nella regolazione della temperatura corporea e nella risposta alla febbre . Un percorso ha origine nel nucleo preottico mediano mentre l'altro ha origine nell'area preottica dorsolaterale (DLPO). Entrambi inibiscono le aree del tronco cerebrale che attivano la termogenesi senza brividi tramite il tessuto adiposo bruno (BAT) in risposta al raffreddore cutaneo o alla prostaglandina E2 .
Ruolo nella termoregolazione
È noto che i mammiferi hanno un ritmo circadiano nella temperatura corporea (Tb) che dipende dall'integrità del nucleo soprachiasmatico (SCN), tuttavia il digiuno influenza anche la Tb nel periodo di riposo e la presenza della SCN è essenziale per questo processo. Sebbene non solo gli SCN ma anche il nucleo arcuato (ARC), siano coinvolti nel setting di Tb attraverso afferenze al nucleo preottico mediano termoregolatorio (MnPO). Dopo gli studi condotti da Guzmán-Ruiz et al. è noto che il rilascio di vasopressina dal SCN abbassa la temperatura appena prima dell'inizio della luce, mentre il rilascio dell'ormone stimolante a-melanociti, soprattutto alla fine del periodo di buio, mantiene alta la temperatura. Entrambi i peptidi hanno effetti opposti sull'attività del tessuto adiposo bruno attraverso nuclei termoregolatori come il nucleo dorsomediale dell'ipotalamo e il nucleo dorsale del rafe. Il coordinamento tra la segnalazione circadiana e quella metabolica all'interno dell'ipotalamo è essenziale per un adeguato controllo della temperatura. L'equilibrio tra i rilasci di neuropeptidi derivati dall'orologio biologico e da un organo sensoriale metabolico come il nucleo arcuato, sono essenziali per un adeguato controllo della temperatura. Queste osservazioni mostrano che le aree cerebrali coinvolte nelle funzioni circadiane e metaboliche del corpo devono interagire per produrre una disposizione coerente dei processi fisiologici associati al controllo della temperatura. [11]
I meccanismi di attivazione neurale coinvolti nella regolazione della temperatura corporea sono in gran parte indefiniti. È noto che le vie simpatiche sono coinvolte nell'aumento della produzione di calore e nella riduzione della perdita di calore e sono attivate dai neuroni nel raphe midollare rostale (RMR). È stato identificato che questi neuroni svolgono un ruolo importante nell'elevazione della temperatura corporea durante l'esposizione al freddo e la febbre indotta dall'osservazione che l' iperpolarizzazione prima dell'esposizione a queste condizioni inibisce l'innalzamento della temperatura corporea in risposta.
Risposta febbrile
Gli input all'RMR dal nucleo preottico mediano sono GABAergici e quindi di natura inibitoria. Le lesioni sul nucleo preottico mediano producono risposte febbrili ridotte , poiché le proiezioni dal MnPn all'RMR contengono i recettori EP3 delle prostaglandine , che sono essenziali per la risposta alla febbre. La prostaglandina E2 si lega ai recettori E3 nel nucleo preottico mediano per inibirne l'attività e causare febbre . Ciò significa che il nucleo preottico mediano è responsabile dei meccanismi inibitori che elevano la temperatura corporea . Questa non è l'unica area dell'ipotalamo coinvolta e l'eliminazione dell'attività del nucleo preottico mediano non causerà di per sé un aumento della temperatura corporea. Tuttavia, se combinato con lesioni su altri nuclei ipotalamici preottici , il danno al nucleo preottico mediano provoca una temperatura corporea basale elevata .
Menopausa
Anche altri recettori, i recettori della neurochinina 3 , che sono espressi nel nucleo preottico mediano, sono coinvolti nella termoregolazione . L'attivazione di questi recettori nei ratti causa una diminuzione della temperatura interna . Questi recettori sono altamente espressi nell'area preottica mediana in risposta alla diminuzione dei livelli di estrogeni nelle donne in menopausa e si ritiene che giochino un ruolo nella generazione di vampate di calore durante la menopausa .
Esposizione al freddo ambientale
Le risposte al freddo sono prodotte da percorsi cutanei sensibili al freddo attraverso l' area parabrachiale . I termocettori nella pelle rilevano la temperatura nell'ambiente rispetto alla temperatura corporea. Questi neuroni afferenti proiettano lungo il midollo spinale fino all'area parabrachiale, che innerva diverse aree dell'area preottica, compreso il nucleo preottico mediano. L'esposizione al freddo porta alla disinibizione dell'RMR e di altre regioni, che porta alla termogenesi dell'adiposo bruno. Questo è anche noto come termogenesi senza brividi, che metabolizza il grasso ma dissipa il calore dalla forza motrice del protone nei mitocondri piuttosto che usare la fosforilazione ossidativa per produrre ATP.
Ruolo nell'osmoregolazione
La regione del cervello che comprende la porzione ventrale del nucleo preottico mediano, il terzo ventricolo anteroventrale (AV3V), è altamente coinvolta nel mantenimento dell'omeostasi di liquidi, elettroliti e cardiovascolari . Il nucleo preottico mediano, insieme all'organo vascolare della lamina terminalis (VOLT) e all'organo subfornicale (SFO) rispondono ai cambiamenti nella composizione del sangue e all'input neurale dai recettori nei vasi sanguigni. Recettori di stiramento della aorta e altri vasi inviano input sensoriale di questa regione, fornendo informazioni sulle volume del sangue e la pressione sanguigna .
Risposta ai cambiamenti nell'osmolalità del sangue
L'importanza del nucleo preoptic mediano composizione fluida e omeostasi può essere visto anatomicamente, in quanto contiene connessioni tra diverse regioni altamente coinvolte nel corpo fluido equilibrio e la funzione cardiovascolare, come il paraventricolare nucleo e supraoptic nucleo.
Funzionalmente, la sua importanza può essere compresa perché le lesioni al nucleo preottico mediano generalmente causano una composizione fluida inappropriata, l'assunzione di acqua e il rilascio di peptide natriuretico atriale (ANP). Le risposte ai cambiamenti nella composizione del fluido mediati dal nucleo preottico mediano derivano dall'innervazione noradrenergica dalle regioni del midollo ventrolaterale caudale. Le risposte possono essere endocrine , autonome o comportamentali e le risposte ai picchi dei livelli di sodio nel sangue includono il rilascio di peptide natriuretico atriale e ossitocina. Il peptide natriuretico atriale viene rilasciato dal cuore in risposta all'ipertensione e all'elevata salinità del sangue. È un vasodilatatore importante e potente e riduce anche la ricaptazione del sodio nei reni. Inoltre, inibisce percorsi come il percorso renina-aldostrone-angiotensina che aumentano la pressione sanguigna .
L'attivazione del nucleo preottico mediano porta alla stimolazione del nucleo paraventricolare (PVN). Le afferenze a quest'area sono glutamatergiche o usano il glutammato come neurotrasmettitore primario, sebbene l' angiotensina II produca una risposta simile e provochi una simpaticoeccitazione del PVN. Ciò è stato confermato dall'uso di un antagonista del recettore del glutammato nel PVN, che ha inibito questa risposta a seguito dell'attivazione del MnPn. Pertanto, il glutammato legato ai recettori è necessario per l' attivazione di questi neuroni nel nucleo preottico mediano e l'attivazione del nucleo paraventricolare. L'attivazione del PVN tramite questo meccanismo glutamatergico si traduce in un aumento dell'attività delle vie nervose simpatiche renali , nonché della frequenza cardiaca e della pressione arteriosa media .
Ruolo nella regolazione omeostatica del sonno
Esperimenti anatomici ed elettrofisiologici su ratti adulti mostrano che un ruolo importante è per il nucleo preottico mediano nella produzione del sonno. La prima prova di ciò è stata l'osservazione che il danno a quest'area ha causato insonnia nei pazienti umani. Esperimenti attuali che utilizzano l' espressione di c-Fos come marker per l'attivazione dei neuroni durante il sonno mostrano una dicotomia di funzione nella promozione e nel mantenimento del sonno tra il nucleo preottico ventrolaterale e il nucleo preottico mediano. L'evidenza suggerisce che i neuroni GABAergici nel nucleo preottico mediano svolgono un ruolo nella promozione dell'inizio del sonno, mentre i neuroni nel nucleo preottico ventrolaterale svolgono un ruolo nel mantenimento del sonno. Mentre l'idea di una completa separazione delle funzioni tra questi due nuclei è attraente, è più probabile che sia una questione di grado di coinvolgimento di questi due nuclei nell'inizio e nel mantenimento del sonno, piuttosto che giocare ruoli completamente separati. È probabile che il MnPn svolga un ruolo importante, ma non esclusivo, nell'insorgenza del sonno, mentre il VLPO gioca un ruolo più importante nel mantenimento del sonno. Entrambe le aree proiettano verso le aree attive del cervello. Esiste anche una proiezione neuronale densa e bidirezionale tra il nucleo preottico mediano e il nucleo preottico ventrolaterale . Questa esistenza di proiezioni inibitorie tra il nucleo preottico ventrolaterno e il nucleo preottico mediano suggerisce una funzione condivisa e una relazione regolatoria tra i due nuclei.
Sonno non REM
La promozione del sonno da parte dei neuroni GABAergici nell'area preottica mediana è più strettamente associata all'NREM , o sonno tranquillo. La quantità di tempo trascorso nel sonno NREM aumenta con il numero di recettori GABA attivati nell'area preottica mediana, come dimostrato dall'aumento del tempo nel sonno NREM in risposta a microiniezioni di agonisti GABA nell'area preottica mediana dei gatti. Il tempo trascorso nel sonno REM non è aumentato e le iniezioni di controllo hanno ridotto il tempo trascorso sia nel sonno NREM che nel sonno REM.
Rapporto con il VLPO
I nuclei ventrolaterale (VLPO) e preottico mediano (MnPn) promuovono il sonno attraverso proiezioni neuronali GABAergiche alle aree del cervello attive nella veglia. L'attivazione dei neuroni nel VLPO e MnPn porta ad un aumento delle concentrazioni del neurotrasmettitore inibitorio primario, GABA, nelle aree di veglia del cervello, come il nucleo tuberomammillare e il locus coeruleus . Ciò porta all'inibizione dell'attività colinergica , noradrenergica e serotoninergica in queste aree. Le proiezioni noradrenergiche dalle aree che promuovono la veglia inibiscono le aree che promuovono il sonno, stabilendo una "interazione inibitoria reciproca" tra le aree del sonno e della veglia che porta alla regolazione dei modelli di sonno . Il meccanismo per l'attivazione dei neuroni promotori del sonno nel VLPO e MnPn non è stato ben definito, tuttavia, è stato suggerito che il nucleo soprachiasmico possa svolgere un ruolo, così come semplicemente diminuito l'input sensoriale all'inizio della sonnolenza.
Riferimenti
[11] Guzmán-Ruiz, MA, Ramirez-Corona, A., Guerrero-Vargas, NN, Sabath, E., Ramirez-Plascencia, OD, Fuentes-Romero, R., ... e Buijs, RM (2015) . Ruolo dei nuclei soprachiasmatici e arcuati nella regolazione della temperatura diurna nel ratto. The Journal of Neuroscience, 35 (46), 15419-15429.